- ホーム
- 政策について
- 政策一覧
- ものづくり/情報/流通・サービス
- バイオ
- 安全審査情報(カルタヘナ法等)
- 規制運用の見直し・改善について(お知らせ)2021年1月
規制運用の見直し・改善について(お知らせ)2021年1月
経済産業省所管事業分野における、産業利用を目的とした遺伝子組換え生物等の閉鎖系使用に係るカルタヘナ法規制運用の見直し・改善について(お知らせ)
平素より、経済産業省の「遺伝子組換え生物等の使用等の規制による生物の多様性の確保に関する法律 (カルタヘナ法)」の執行行政に理解と協力をいただきありがとうございます。
この度経済産業省では、経済産業省所管事業分野における、産業利用を目的とした遺伝子組換え生物等の閉鎖系使用(カルタヘナ法産業二種使用)に係る法規制の執行について、電子申請手続の導入、包括確認申請手続及び審査体制の見直し等、下記の一連の運用見直し・改善を行うこととしましたのでご連絡します。
また、これに伴い、当省所管事業分野におけるカルタヘナ法産業二種使用に係る法令の規定の概要やその解釈、申請書の記載要領含む申請方法、Q&A等をまとめた「遺伝子組換え生物等の使用等の規制による生物の多様性の確保に関する法律 (カルタヘナ法)の解説(申請マニュアル)」の第4版(以下、「申請マニュアル第4版」とします。)を発行します。
併せて、本ウェブサイトについても、より利用しやすくなるようレイアウトの見直しを行うとともに、第二種使用等にあたっての注意点のページや事故等緊急時への備え及び対処のページを作成しました。
今後とも、法規制等を遵守した安全な遺伝子組換え生物等の使用に、理解と協力をいただけるようお願いします。
掲載項目
- (1)申請・審査手続の見直し(包括確認申請手続関係を除く)
- 電子申請手続の導入
- 審査手続の見直しと標準処理期間の短縮
- (2)包括確認申請手続の見直し
- 供与核酸の対象範囲
- 申請者要件の見直し
- 申請手続に関する記載の追加
- 現場確認の実施
- 包括確認を受けた使用者への要求事項等
- (4)関連の通知・マニュアルの改正
(1)申請・審査手続の見直し(包括確認申請手続関係を除く)
電子申請手続の導入
利用者の利便性向上の観点から、e-Govを利用した電子申請手続による申請書等の受付を開始しました。
対象は、以下4手続になります。
1)第二種使用等拡散防止措置確認申請
2)申請書記載事項変更届
3)包括確認申請手続の利用に係る遺伝子組換え生物等の使用実績等報告届
4)GILSP告示への掲載希望届
電子申請手続の詳細については、こちらをご確認ください。
審査手続の見直しと標準処理期間の短縮
これまで申請書が正式に提出される前にNITEが事前審査を行っていたものを、申請書の提出後に経済産業省及びNITEが審査する形に改めることで、電子申請手続による場合の標準処理期間を短縮(4週間→3週間)しました。
変更届(申請書記載事項変更届)の対象の見直し
培養工程の追加等の場合であっても再申請ではなく変更届で対応可能とするなど、変更届の対象を拡大しました。
また、安全委員会の構成員変更については届出不要としました。
なお、変更内容に問題がないことについては経済産業省及びNITEで審査を行います。
変更届の詳細については、こちらをご確認ください。
(2)包括確認申請手続の見直し
以下の見直しを行うべく、平成30年1月11日付通知「包括申請における拡散防止措置の確認について」(20171220商局第1号)を改正し、「包括確認申請手続による拡散防止措置の確認について(通知)」(20201125商局第2号)![]() を令和3年1月22日付で制定しました。
を令和3年1月22日付で制定しました。
改正内容の詳細は以下をご確認ください。また、包括確認申請手続の詳細については、こちらをご確認ください。
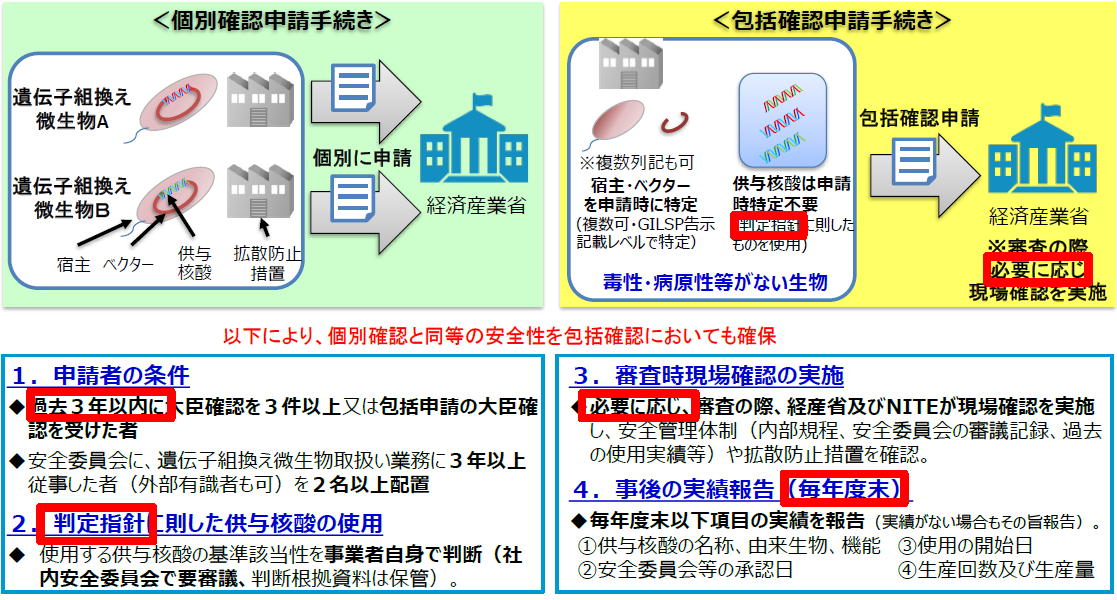
包括確認申請手続きイメージ(改正後)
包括確認申請手続きイメージ(改正前)
改正項目
供与核酸の対象範囲
宿主、ベクター及び遺伝子組換え微生物については産業二種省令様式第一備考17a(以下、「備考17a」という。)のGILSPの基準を満たすことを求める一方、供与核酸についてはこれとは異なる基準を設定しておりました(下表改正前(2)参照)。
今回の見直しにより、本申請手続による確認で利用可能となる遺伝子組換え生物を、備考17aに定められているGILSPの基準を満たす遺伝子組換え微生物と一致させることとしました。(下表改正後参照)
なお、これにより供与核酸のGILSP基準該当性の判断は備考17a(2)に従うことになるため、供与核酸判定指針を廃止することとしました。
改正前 |
改正後 |
|---|---|
第1 包括申請の対象範囲 |
第1 包括確認申請手続による確認で利用可能となる遺伝子組換え生物 |
申請者要件の見直し
申請者については申請の日以前「3年以内に個別に確認3件以上」受けていることを要件としていましたが、「3件以上(他省庁所管分野を含む)」個別に第二種使用等の大臣確認を受けた実績を申請者要件とするよう、見直すこととしました。
なお、安全委員会の構成員に変更が生じる場合には変更届の提出を不要としますが、継続して遺伝子組換え微生物の取扱業務等に3年以上従事した経験を要する者を2名以上配置するとの要件が満たされるようにすることを求める旨明記しました。
改正前 |
改正後 |
|---|---|
第2 確認の基準 |
第2 包括確認申請手続の申請者要件 |
申請手続に関する記載の追加
平成30年1月11日付通知では申請手続についての規定がなく今回明記することとしました。(なお、申請手続そのものに変更はございません。)
改正後(新規) |
|---|
第3 申請手続 |
現場確認の実施
包括確認申請手続における審査においては、「必要と認めるとき」に現場確認を行うこととしておりましたが、今回の見直しに対しより慎重を期す観点、また、一定の範囲の遺伝子組換え生物等の第二種使用等に係る拡散防止措置の包括的な確認を行うに当たっては、現場をしっかりと確認しておくことが肝要との観点から、「原則として」現場確認を実施することとしました。
なお、申請の日以前に別の遺伝子組換え生物等の使用等で包括確認を受けている場合や、法第31条又は法第32条に基づく立入検査を実施している場合、この他、既に必要な現場の確認ができていると経済産業省及びNITEが判断する場合には、現場確認を実施しないことがあります。
改正前 |
改正後 |
|---|---|
第3 経済産業大臣による確認の手続 |
第4 審査における現場確認の実施 |
包括確認を受けた使用者への要求事項等
使用実績の報告は、毎年度末ではなく、毎年度終了後速やかに報告いただくように、また、理解しやすさの観点から規定ぶりを改めました。
使用する供与核酸がGILSPの基準に該当することを経済産業省が事前に確認していることについて、明示的な根拠の提出を求められる場合がある(他省庁所管領域で使用する場合等)ことから、使用実績等報告書の提出によってこれを確認する措置を含めることとしました(改正後(3)参照)。
改正前 |
改正後 |
|---|---|
第4 包括確認を受けた者の行動指針 |
第5 包括確認を受けた遺伝子組換え微生物の使用に当たっての要求事項等 |
改正に係る経過措置の追加
過去に包括確認申請手続により大臣確認を受けている場合には、本改正通知に則って遺伝子組換え生物等を使用することとし、供与核酸についても、本改正通知第1の基準を満たすものを変更届の提出等特段の手続を経ずとも使用できるものとする旨明記しました。
改正後(新規) |
|---|
第6 過去に包括確認申請手続により大臣確認を受けている場合 |
(3)バキュロウイルス生産系を用いて生産された試薬の取扱い見直し
バキュロウイルス生産系を用いて生産された試薬のうち、アフィニティ精製を経たものについてはカルタヘナ法規制非対象品として扱うことができる旨FAQ(Q1-17)に明記しました。(詳細はこちら)
(4)関連の通知・マニュアルの改正
以上の運用見直しに係る 「第二種使用等に係る大臣確認手順及びチェックリスト(お知らせ)」の改正を行いました。
詳細については同お知らせ、本ウェブサイト又は申請マニュアル第4版をご確認ください。
/以上
お問合せ先
<経済産業省の連絡先・問い合わせ先等>経済産業省 商務・サービスグル-プ 生物化学産業課
生物多様性・生物兵器対策室(カルタヘナ法執行担当)
住所:〒100-8901
東京都千代田区霞が関1-3-1
TEL:03-3501-8625(直通)
E-mail : bzl-cartagena@meti.go.jp
https://www.meti.go.jp/policy/mono_info_service/mono/bio/cartagena/anzen-shinsa2.html
<NITEの連絡先・問い合わせ先等>
独立行政法人 製品評価技術基盤機構(NITE)バイオテクノロジーセンター
生物多様性支援課(カルタヘナ法執行・支援担当)
住所:〒151-0066
東京都渋谷区西原2-49-10
TEL:03-6674-4668
E-mail : nite-cartagena@nite.go.jp
https://www.nite.go.jp/nbrc/cartagena/index.html
最終更新日:2023年3月8日